Operaciones unitarias: Mecanismos de transferencia de calor
Mecanismos de transferencia de calor
Siempre se realiza cuando existe una diferencia de temperatura y el mecanismo de esta transferencia de calor se divide en:
- Conducción
- Convección
- Radiación
Conducción
Para que haya conducción se requiere un medio material continuo que no esté vacío. Si existe un gradiente de temperatura, el calor fluye en un sentido decreciente de mayor a menor temperatura. Esto no implica que existe simultáneamente ningún desplazamiento de materia a nivel macroscópico. Este fenómeno recibe el nombre de conducción molecular. Si el medio material son gases o líquidos, puede producirse un desplazamiento a nivel molecular de moléculas individuales. En el caso de que sean sólidos metálicos, a nivel molecular se produce por electrones libres. Si son iones sólidos se produce por la vibración de los iones o moléculas que constituyen el sólido.
Convección
Un fluido, como consecuencia de tener una masa y una velocidad, puede transportar una cantidad de movimiento. Además, en virtud de su temperatura, es capaz de portar una energía. Estrictamente hablando la convección es el transporte de energía por movimiento del medio.
En ingeniería hay una explicación más general del término convección. Convección se emplea con el fin de incluir la transferencia de calor desde una superficie a un fluido que se encuentra en movimiento. A este fenómeno se le denomina transferencia de calor por convección. Esta convección puede ser natural o forzada.
En el caso de la natural solo actúan fuerzas de flotación en el fluido, las cuales están generadas por las diferencias de densidades que aparecen en el fluido. Las forzadas aparecen cuando ponemos dispositivos mecánicos que comunican al fluido energía poniéndole en movimiento; los dispositivos mecánicos pueden ser bombas, agitadores …
Un sólido solo puede recibir o transmitir calor por conducción. En la conducción se requería una transmisión de calor a nivel molecular, mientras que en la convección está basada en el movimiento del fluido.
Radiación
La emisión por radiación se realiza por ondas electromagnéticas. Si la radiación se realiza en el vacío, no se transformará en calor ni en ninguna otra forma de energía. Pero si la radiación incide sobre un medio material, y es absorbida por él, la radiación se transforma en calor y estará suministrando energía al medio material pudiendo producir reacciones fotoquímicas o cualquier otro fenómeno.
Se estudia separadamente de la conducción y convección. El fenómeno de la radiación solo tiene importancia a nivel industrial a elevadas temperaturas.
Aparatos utilizados en la transferencia de calor
Los aparatos que se utilizan tienen que ver con el aislamiento térmico, calentamiento o enfriamiento de fluidos y con la evaporación y condensación y con los mecanismos que se utilizan.
| Operaciones | Conducción | Convección | Radiación |
|---|---|---|---|
| Aislamiento térmico | Aislantes/refractarios | Camisas de vacío | Espejos de radiación |
| Calentamiento o enfriamiento de fluidos | Intercambiadores de calor/placas solares | Hornos | |
| Evaporación | Evaporadores | ||
| Condensación | Condensadores | ||
Los que tienen mayor aplicación son los intercambiadores de calor, que son aparatos cuyo objetivo es crear una corriente de fluido a una determinada temperatura. Para lograr esto se calienta o refrigera dicha corriente.
Los fluidos (líquido, gas) circulan a través de una superficie en la cual intercambian el calor. Dentro de una instalación, en los intercambiadores de calor se dan varios procesos a la vez como consecuencia de que se emplea la refrigeración de unos para el calentamiento de otros (se minimiza el gasto de energía).
Se emplean en refrigeraciones petroquímicas.
Los factores que se deben considerar en la elección de un intercambiador de calor son:
- Temperatura a la que se trabaja
- Estado del fluido (vapor o líquido)
- Presión a la que se someten los fluidos
- Pérdidas de presión en los intercambiadores
- Caudal del fluido (vol/s)
- Acción corrosiva del fluido tratado
- Posibilidad del sistema de ensuciarse, que supone pérdida de calor
- Tamaño posible de la instalación
Tipos de intercambiadores de calor
1. Intercambiadores de calor de doble tubo:
Constituidos por dos tuberías concéntricas, por cada una de ellas circula un fluido. El intercambio de calor tiene lugar a través de la pared que pone en contacto a ambos fluidos. Esto solo se utiliza cuando se requiere poco intercambio de calor.
2. Intercambiadores de calor de carcasa y tubos:
Son los más utilizados, están compuestos por una superficie, dentro de la cual hay muchos tubos de menor diámetro que se encuentran en paralelo al eje del cilindro que constituye la carcasa.
Los tubos concéntricos están unidos entre si y además hacemos circular un fluido por el interior de los tubos, mientras que un segundo fluido está bañando a los tubos con lo que el intercambio de calor es más efectivo que en el caso anterior.
Los tubos están formados por materiales metálicos, pero si queremos transportar fluidos corrosivos se sustituyen por materiales plásticos polifluorados.
Los tubos se sustituyen por superficies planas con rugosidades cuando se pueden formar precipitados.
3. Intercambiadores de calor por grafito:
Se emplean para líquidos muy corrosivos. Están constituidos por carbono grafito taladrado. Sobre la superficie del grafito es donde se produce el intercambio de calor. El grafito suele estar prensado.
Hornos
Son dispositivos en los que un sólido o un fluido se calientan básicamente por radiación mediante la combustión en un recinto cerrado de un combustible cualquiera. Puede ser carbón, un líquido (fuel-oil), o un gas (gas natural).
Condensadores
Tienen el objetivo de condensar un vapor mediante un líquido frío. Los aparatos son muy parecidos a los intercambios de calor, en los que el agua que sirve para refrigerar se suele introducir por medio de una pulverización que cae sobre los tubos.
Evaporadores
También hay intercambio de calor que conlleva un cambio de fase. El objetivo es concentrar una disolución y también obtenerse vapor del disolvente. A nivel industrial tienen una doble finalidad:
- Obtener el líquido condensado: leche condensada
- Obtener el vapor: desalinizadores
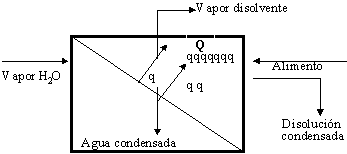
Se concatenan evaporadores para ahorrar energía al aprovechar el calor del vapor para calentar el alimento del siguiente.
Placas solares
Conjugan las tres maneras de conducción de calor.
El serpentín ha de estar pintado de negro para poder absorber la radiación. La radiación atraviesa el cristal sin ningún efecto, incide sobre el serpentín y aumenta el calor produciendo el efecto invernadero. La radiación absorbida no puede salir por el cristal, por ello aumenta la temperatura, produciéndose una transmisión de calor al líquido que va atravesando el serpentín. Esta transmisión de calor se produce de una forma combinada de conducción y convección.
Hay 3 formas de perder calor en este sistema:
- A través del cristal: cesión por conducción
- Por medio del contacto con el aire exterior: por convección
- Pérdida por conducción en el soporte
O.U.F. regidas por transferencia simultánea de Q y materia (contacto entre fases y directo)
Puede darse que al poner en contacto 2 fases entre si se de un intercambio de materia y calor en sentidos contrarios.
Acondicionamiento de gases o enfriamiento de líquidos
El gas suele ser el aire y el líquido el agua pero el fundamento es universal. Es la operación unitaria que tiene por objeto modificar las condiciones de humedad y temperatura de una corriente de aire por interacción directa con otra corriente de agua. También se suele hablar de humidificar el aire, deshumidificar el aire, enfriamiento del agua.
La humidificación se consigue poniendo en contacto aire no saturado con una corriente de agua a unas temperaturas en las que el aire aumente su contenido en humedad.
La deshumidificación se conseguirá al poner en contacto aire húmedo con un líquido más frío; de esta manera conseguiremos que se condense el agua que había en el aire y por lo tanto disminuya su contenido en agua inicial. De esta manera obtendremos un valor deseado de humedad absoluta. A continuación el aire lo puedo calentar al valor que deseemos y este es el funcionamiento de los acondicionadores de aire que se utilizan actualmente.
A nivel industrial se emplea el enfriamiento de agua colocando una cantidad muy grande de maderas en las que se pulveriza el agua por la parte superior y el aire se introduce a presión por unas toberas. El) Problema que tiene es que se producen pérdidas de agua en el gas húmedo, por lo que hay que suministrar ese caudal.
Tenemos una disolución con una cierta presión de vapor que está en contacto con aire con una cierta humedad. Puede ocurrir que la presión de vapor del agua de la disolución sea mayor o menor que la del aire. Dependiendo esto tendremos un fenómeno u otro.
Si la presión de vapor de la disolución es mayor que la del aire entonces pasa agua al aire; la disolución se hace más concentrada al haber menos disolvente. Llega un momento que al bajar la presión de vapor de la disolución se iguala a la del aire y se obtiene el fenómeno.
Si la presión de vapor del aire es mayor que la de la disolución, el agua del aire condensa en la disolución y esta se hace más diluida y la presión de vapor de la disolución aumenta hasta igualarse con el aire.
Delicuescencia
Sustancias sólidas que tienen una elevada solubilidad en agua. Tenemos un sólido en contacto con humedad. En la superficie del sólido se forma una película que absorbe agua hasta que se satura. Si la disolución es saturada tendrá una presión de vapor muy pequeña y atraerá mayor cantidad de agua del aire. Esas nuevas moléculas van a seguir disolviendo el sólido y llegará un momento en que todo el sólido pasa a líquido (disolución). El sólido llega a convertirse en líquido.
Higroscopía
Sustancias que tienen tendencia a coger moléculas de agua pero sin llegar a disolverse. Todas las sustancias delicuescentes son higroscópicas pero no al revés.
Eflorescencia
Sólidos con moléculas de agua de cristalización, en atmósfera seca parte de las moléculas pasan al aire.
Cristalización
Formación de partículas sólidas cristalinas en el seno de una fase homogénea. Desde el punto de vista industrial la cristalización más importante es la que conlleva la formación de cristales a partir de disoluciones líquidas sobresaturadas. Sus objetivos son:
- Formar sustancias con presentación más agradable
- Grado de pureza
Características:
- Tamaño
- Forma
- Uniformidad
- Pureza
Las tres primeras son propias de la cristalización. La pureza depende además de la disolución en el disolvente, es decir, recristalización.
En toda formación de cristales hay que considerar dos etapas:
Nucleación: formación de los primeros iones a partir de los iones o moléculas que se encuentran en el seno de la disolución. Puede ser que estos primeros cristales que se forman, se destruyan debido a un proceso inverso a la nucleación.
Crecimiento: formación de la estructura cristalina.
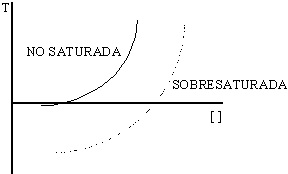
Es fundamental el estudio de la variación de las curvas de la temperatura frente a la concentración (solubilidad).
Si colocamos un cristal en una zona no saturada, se destruye. Para disolver un sólido hay que administrar calor normalmente, por lo tanto la temperatura bajará un poco.
Si ponemos un cristal en una zona de sobresaturación, el cristal crece mucho pero no se forman nuevos cristales.
Si trabajamos en la zona metaestable (lo más cerca posible de la sobresaturación) se forman nuevos cristales. El) Problema es que la curva de sobresaturación no está bien definida.
Cristalizadores:
- Tanque: la sobresaturación se produce por enfriamiento de la disolución. Se emplea cuando la solubilidad de la sustancia a cristalizar varían mucho con la temperatura
- Evaporadores: se produce la cristalización por medio de la evaporación, se utiliza cuando la solubilidad de la sustancia varía poco con la temperatura
- De vacío: se combina la evaporación con el enfriamiento. Se emplea cuando se quiere trabajar a baja temperatura y con rapidez
Cuando tengo una sal disuelta en agua (considero solo el líquido y el sólido) y bajo la temperatura, se produce la aparición de un precipitado hasta un momento en el cual toda la disolución pasa a fase sólida (mezclas eutécticas). Este punto es característico de cada mezcla; por debajo de la temperatura eutéctica no se encuentra fase líquida. Estos diagramas eutécticos son muy similares a los de las aleaciones pero en estas últimas ocurre al contrario pero en este caso es al contrario.
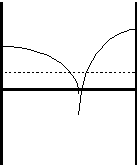
(1) Punto eutéctico, por debajo de él todo está en fase sólida. Por encima de las curvas trabajo en fase líquida.
A: punto de congelación del agua.
C: punto congelación de la sal.
B: punto eutéctico.
En el punto P tengo una disolución diluida, si bajo la temperatura hasta el punto P' empieza a aparecer un sólido (hielo), si bajo hasta P" la composición de la disolución sigue la curva P'D va desapareciendo el agua pero tengo la misma cantidad de sólido. En P‴ tenemos un punto eutéctico y por tanto sólo tendremos sólido, pero tenemos dos fases, una de hielo y otra fase con la composición del eutéctico.
Si estudiamos a partir del punto 2 es igual pero en vez de tener agua en fase sólida, tengo sal precipitada y en el punto eutéctico tendré un sólido que es sal y otro sólido con la composición del punto eutéctico.
1 + L = 2 + 2 ⟶ L = 3 Para encima de la curva.
Como P = constante L = 3-1 ⟶ L = 2 Temperatura, composición.
Para la zona por debajo de la curva:
L + 2 = 2 + 2 ⟶ L = 2
L - 1 ⟶ L = 1 Elijo la temperatura y obtengo la composición o inversa.
En el punto eutéctico L = 0, no tengo ningún grado de libertad, es característico de cada disolución.
Puedo conocer la composición de sólido y líquido en cada zona mediante la línea de interconexión.
1) NH2O liq./NH2O sol. = EF/FD
2) Nsal liq./Nsal sol. = HI/GH
En el caso de las aleaciones se trabaja igual pero con temperatura de ebullición.
Secado
Operación unitaria física regida por la transferencia simultánea. Su objetivo es reducir el contenido de agua de un sólido. En algunas ocasiones es el punto final para conseguir un producto listo para el envasado.
Si tengo un sólido con mucha agua intento eliminarla mediante medios mecánicos y esto es previo al secado pero no es el secado. El término secado indica la disminución de la humedad del sólido. Todo el agua del sólido no tiene las mismas características. Un sólido tendrá mayor o menor cantidad de agua según la hidroscopía que presente este sólido.
Agua ligada: suponemos que la presión de vapor ligada al sólido es menor a la que corresponde a cuando está libre.
Agua libre: si presenta una presión de vapor determinada para la temperatura a la que trabajo.
Pongo en contacto el sólido con aire húmedo y vemos que nunca consigo quitar el agua ligada del sólido.
Operación unitaria química
Tiene por objetivo distribuir de una forma distinta los átomos de una molécula para dar otra, es decir, el paso de los reactivos a los productos. Se da en los reactores químicos; para el diseño de estos se deben estudiar estas características:
- Asegurarnos de que el modo de fluir de los reactivos sea total, para conseguir la mezcla deseada
- Proporcionar el tiempo de contacto necesario entre las sustancias y el catalizador (si lo hay) hasta lograr la extensión deseada de la reacción
- Permitir que se adquieran las condiciones de presión, temperatura y composición de modo que la reacción tenga lugar en el modo y la velocidad deseadas, para lo cual hay que atender a los aspectos termodinámicos y cinéticos de la reacción
Modelos de flujo
Son las formas en que se ponen en contacto los fluidos en el reactor químico. Existen dos grandes tipos de modelos de flujos que son ideales, en la realidad nunca se dan pero sirven de referencia:
- Modelo de mezcla perfecta: lo que se consigue es que exista una homogeneidad perfecta en la reacción, todos los puntos han de tener la misma temperatura y presión, consiguiendo que toda la mezcla que se extraiga tendrá idénticas condiciones a la que está en el interior del reactor
- Modelo de flujo en pistón (de flujo tapón): se basa en que el fluido entra sin haber cambios de concentración a lo largo del eje en que se mueven los reactivos. El tiempo de permanencia en el reactor es el mismo para todos los componentes. En cada uno de los cambios los reactivos tienen la misma temperatura y composición en cada punto a lo largo del reactor
Todos los modelos que se diseñan de reactores químicos están basados en uno de estos dos modelos de flujo.
El modelo de mezcla perfecta da lugar a un reactor de tanque agitado.
El modelo de pistón o tapón da lugar a un reactor tubular.
En el reactor de tanque agitado es muy difícil obtener la homogeneidad en el interior ya que aparecen caminos preferentes. En el reactor tubular las interacciones con todas las zonas es muy difícil ya que hay reacciones radiales.
Reactores químicos
Los más importantes son los anteriormente citados. Dentro de los reactores de tanque agitado en los que se puede trabajar de forma contínua o discontínua obteniendo producciones pequeñas y medianas ya que la velocidad no es muy grande, se puede trabajar en un amplio rango de temperatura y presión, y permiten trabajar con o sin reflujo. Son un recipiente donde se encuentra un fluido (reaccionante) y se eliminan del sistema, se puede controlar la presión y la temperatura del sistema. Para regular la temperatura:
- Colocación de camisas de vapor
- Colocando un serpentín
- Método de la recirculación exterior del líquido. Colocando un calentador que hace circular un líquido que recircula una vez que se ha enfriado
Estos reactores se emplean para reacciones homogéneas de líquido, también cuando los reactivos son líquidos y dan lugar a un sólido. También se emplean cuando los reactivos son líquidos menos uno que es un gas que se hace borbotear en el líquido.
Los reactores tubulares se emplean cuando trabajo con reactivos en fase gaseosa. En ellos es frecuente la presencia de catalizadores que normalmente se encuentran en fase sólida. Tenemos una catálisis heterogénea. El diseño de estos reactores depende de la exotermicidad del proceso y también del tiempo de residencia necesario en el interior del reactor.
• Reactores tubulares calentados a fuego directo: consiste en tubos colocados en un horno, la reacción tiene lugar en el interior de los tubos y va catalizada
• Reactores tubulares de carcasa y tubos: son similares a los intercambiadores de calor de carcasa y tubos, la reacción tiene lugar en el interior de los tubos y circulando por el intermedio un refrigerante o un calefactor para conseguir la temperatura adecuada, también pueden usar catalizadores
• Reactores tubulares de lecho: (fijo, móvil, fluilizado)
1) El catalizador es fijo ya que ocupa una posición dada en el espacio. Lo normal es colocar varias capas de catalizadores a diferentes alturas y entre ellas existen intercambiadores de calor
2) En los de lecho móvil las partículas se mueven continuamente del reactor a un recipiente anexo donde se limpia y regenera el catalizador. Se emplea cuando hay reacciones muy exotérmicas también se emplean cuando la reacción da productos no deseados que contaminan el catalizador e inhiben su acción
3) En los de lecho fluilizado las partículas del catalizador tienen un movimiento mucho más libre, son menos compactas. Se emplean en la industria petroquímica. Suele haber varias capas y en medio existe refrigeración o calefacción
• Reactores de hornos rotatorios: se emplean en la industria del cemento. Son una variante de los tubulares. El sólido avanza por el tubo gracias a una cierta inclinación. Todos los componentes son sólidos. La inclinación va acompañada de una rotación. Se emplean altas temperaturas
• Reactores biológicos: intervienen organismos vivos. Base de la biotecnología. Dentro de ellos tenemos los autoclaves o fermentadores (reactores tanque agitado)
• Reactores electroquímicos: La energía se da en forma de corriente eléctrica contínua, en los electrodos se obtienen los productos de reacción
Autor: Sin datos
Editor: Ricardo Santiago Netto (Administrador de Fisicanet)
- ‹ Anterior
- |
- Siguiente ›