Fuentes de energía no renovables
Fuentes de Energía No Renovables
Son fuentes de energía no renovables aquellas que se encuentran en forma limitada en nuestro planeta y se agotan a medida que se les consume.
Son fuentes de energía no renovables:
- Carbón
- Petróleo
- Gas natural
- Energía geotérmica
- Energía nuclear
El Carbón
Es un combustible fósil, formado por la acumulación de vegetales durante el Período Carbonífero de la era Primaria de nuestro planeta. Estos vegetales a lo largo del tiempo han sufrido el encierro en el subsuelo terrestre, experimentando cambios de presión y temperatura lo que ha posibilitado la acción de reacciones químicas que los han transformado en variados tipos de carbón mineral.
El Petróleo
Es un aceite natural de origen mineral constituido por una mezcla de hidrocarburos. Estos hidrocarburos se producen por antiguos restos de organismos vegetales, organismos acuáticos y organismos vivos depositados en las profundidades de la corteza terrestre en forma de sedimentos.
El Gas Natural
Es una mezcla de gases combustibles depositados en forma natural en el subsuelo de la Tierra y que poseen un gran poder calorífico. En ocasiones los yacimientos de gas natural se encuentran acompañados por yacimientos de petróleo.
El principal componente del gas natural es el metano y en menor proporción los gases de etano, propano y butano.
Energía Geotérmica
Energía contenida también en el interior de la Tierra en forma de gases. Al ser extraída se presenta en forma de gases de alta temperatura (fumarolas), en forma de vapor y agua hirviendo (géiser) y en forma de agua caliente (fuentes termales).
Energía Nuclear
La energía nuclear es aquella que se libera como resultado de una reacción nuclear. Se puede obtener por el proceso de fisión nuclear (división de núcleos atómicos pesados) o bien por fusión nuclear (unión de núcleos atómicos muy livianos). En las reacciones nucleares se libera una gran cantidad de energía, debido a que parte de la masa de las partículas involucradas en el proceso, se transforma directamente en energía. Lo anterior se puede explicar en base a la relación masa-energía, producto de la genialidad del gran físico Albert Einstein.
En relación a la liberación de energía, una reacción nuclear es un millar de veces más energética que una reacción química, por ejemplo, la generada por la combustión del combustible fósil del metano.
Fisión Nuclear
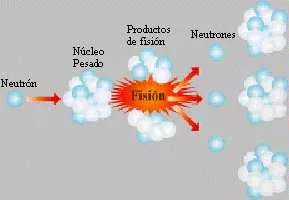
Es una reacción nuclear que tiene lugar por la rotura de un núcleo pesado al ser bombardeado por neutrones de cierta velocidad. A raíz de esta división el núcleo se separa en dos fragmentos acompañado de una emisión de radiación, liberación de 2 ó 3 nuevos neutrones y de una gran cantidad de energía (200 MeV) que se transforma finalmente en calor.
Los neutrones que escapan de la fisión, al bajar su energía cinética, se encuentran en condiciones de fisionar otros núcleos pesados, produciendo una reacción nuclear en cadena. Cabe señalar, que los núcleos atómicos utilizados son de Uranio - 235.
El proceso de la fisión permite el funcionamiento de los reactores nucleares que actualmente operan en el mundo.
Fusión Nuclear
La fusión nuclear ocurre cuando dos núcleos atómicos muy livianos se unen, formando un núcleo atómico más pesado con mayor estabilidad. Estas reacciones liberan energías tan elevadas que en la actualidad se estudian formas adecuadas para mantener la estabilidad y confinamiento de las reacciones.
La energía necesaria para lograr la unión de los núcleos se puede obtener utilizando energía térmica o bien utilizando aceleradores de partículas. Ambos métodos buscan que la velocidad de las partículas aumente para así vencer las fuerzas de repulsión electrostáticas generadas al momento de la colisión necesaria para la fusión.
Para obtener núcleos de átomos aislados, es decir, separados de su envoltura de electrones, se utilizan gases sobrecalentados que constituyen el denominado Plasma Físico. Este proceso es propio del Sol y las estrellas, pues se tratan de gigantescas estructuras de mezclas de gases calientes atrapadas por las fuerzas de gravedad estelar.
El confinamiento de las partículas se logra utilizando un "Confinamiento Magnético", o bien un "Confinamiento Inercial". El Confinamiento Magnético aprovecha el hecho que el plasma está compuesto por partículas (núcleos) con carga eléctrica. Se sabe que si una de estas partículas interactúa con un Campo Magnético su trayectoria y velocidad cambian, quedando atrapadas por dicho Campo. El Confinamiento Inercial permite comprimir el plasma hasta obtener densidades de 200 a 1.000 veces mayor que la de sólidos y líquidos. Cuando se logra la compresión deseada se eleva la temperatura del elemento, lo que facilita aún más el proceso de la fusión.
La fusión nuclear se puede representar por el siguiente esquema y relación de equilibrio:
²H + ²H ⟶³He + ¹n + 3,2 MeV
Elementos de física nuclear
Un Poco de Historia
Cinco siglos antes de Cristo, los filósofos griegos se preguntaban si la materia podía ser dividida indefinidamente o si llegaría a un punto que tales partículas fueran indivisibles. Es así, como Demócrito fórmula la teoría de que la materia se compone de partículas indivisibles, a las que llamó átomos (del griego átomos, indivisible).
En 1.803 el químico inglés John Dalton propone una nueva teoría sobre la constitución de la materia. Según John Dalton toda la materia se podía dividir en dos grandes grupos: los elementos y los compuestos. Los elementos estarían constituidos por unidades fundamentales, que en honor a Demócrito, John Dalton denominó átomos. Los compuestos se constituirían de moléculas, cuya estructura viene dada por la unión de átomos en proporciones definidas y constantes. La teoría de Dalton seguía considerando el hecho de que los átomos eran partículas indivisibles.
Hacia finales del siglo XIX, se descubrió que los átomos no son indivisibles, pues se componen de varios tipos de partículas elementales. La primera en ser descubierta fue el electrón en el año 1.897 por el investigador Joseph John Thomson, quién recibió el Premio Nobel de Física en 1.906. Posteriormente, Hantaro Nagaoka (1.865 - 1.950) durante sus trabajos realizados en Tokio, propone su teoría según la cual los electrones girarían en órbitas alrededor de un cuerpo central cargado positivamente, al igual que los planetas alrededor del Sol. Hoy día sabemos que la carga positiva del átomo se concentra en un denso núcleo muy pequeño, en cuyo alrededor giran los electrones.
El núcleo del átomo se descubre gracias a los trabajos realizados en la Universidad de Manchester, bajo la dirección de Lord Ernest Rutherford of Nelson entre los años 1.909 a 1.911. El experimento utilizado consistía en dirigir un haz de partículas de cierta energía contra una plancha metálica delgada, de las probabilidades que tal barrera desviara la trayectoria de las partículas, se dedujo la distribución de la carga eléctrica al interior de los átomos.
Constitución del Atomo y Modelos Atómicos
La descripción básica de la constitución atómica, reconoce la existencia de partículas con carga eléctrica negativa, llamados electrones, los cuales giran en diversas órbitas (niveles de energía) alrededor de un núcleo central con carga eléctrica positiva. El átomo en su conjunto y sin la presencia de perturbaciones externas es eléctricamente neutro.
El núcleo lo componen los protones con carga eléctrica positiva, y los neutrones que no poseen carga eléctrica.
El tamaño de los núcleos atómicos para los diversos elementos están comprendidos entre una cienmilésima y una diezmilésima del tamaño del átomo.
La cantidad de protones y de electrones presentes en cada átomo es la misma. Esta cantidad recibe el nombre de número atómico, y se designa por la letra Z. A la cantidad total de protones más neutrones presentes en un núcleo atómico se le llama número másico y se designa por la letra A.
Si designamos por X a un elemento químico cualquiera, su número atómico y másico se representa por la siguiente simbología:
ZXA
Por ejemplo, para el hidrógeno tenemos: ₁H¹.
Si bien, todas las características anteriores de la constitución atómica, hoy en día son bastante conocidas y aceptadas, a través de la historia han surgido diversos modelos que han intentado dar respuesta sobre la estructura del átomo. Algunos de tales modelos son los siguientes:
a) El Modelo de Thomson
Thomson sugiere un modelo atómico que tomaba en cuenta la existencia del electrón, descubierto por él en 1.897. Su modelo era estático, pues suponía que los electrones estaban en reposo dentro del átomo y que el conjunto era eléctricamente neutro. Con este modelo se podían explicar una gran cantidad de fenómenos atómicos conocidos hasta la fecha. Posteriormente, el descubrimiento de nuevas partículas y los experimentos llevado a cabo por Ernest Rutherford demostraron la inexactitud de tales ideas.
b) El Modelo de Rutherford
Basado en los resultados de su trabajo que demostró la existencia del núcleo atómico, Rutherford sostiene que casi la totalidad de la masa del átomo se concentra en un núcleo central muy diminuto de carga eléctrica positiva. Los electrones giran alrededor del núcleo describiendo órbitas circulares. Estos poseen una masa muy ínfima y tienen carga eléctrica negativa. La carga eléctrica del núcleo y de los electrones se neutralizan entre sí, provocando que el átomo sea eléctricamente neutro.
El modelo de Rutherford tuvo que ser abandonado, pues el movimiento de los electrones suponía una pérdida contínua de energía, por lo tanto, el electrón terminaría describiendo órbitas en espiral, precipitándose finalmente hacia el núcleo. Sin embargo, este modelo sirvió de base para el modelo propuesto por su discípulo Niels Henrik David Bohr, marcando el inicio del estudio del núcleo atómico, por lo que a Rutherford se le conoce como el padre de la era nuclear.
c) El Modelo de Bohr
El físico danés Neils Bohr (Premio Nobel de Física 1.922), postula que los electrones giran a grandes velocidades alrededor del núcleo atómico. Los electrones se disponen en diversas órbitas circulares, las cuales determinan diferentes niveles de energía. El electrón puede acceder a un nivel de energía superior, para lo cual necesita "absorber" energía. Para volver a su nivel de energía original es necesario que el electrón emita la energía absorbida (por ejemplo en forma de radiación). Este modelo, si bien se ha perfeccionado con el tiempo, ha servido de base a la moderna física nuclear.
d) Modelo Mecano - Cuántico
Se inicia con los estudios del físico francés Prince Louis-Victor Pierre Raymond de Broglie, quién recibió el Premio Nobel de Física en 1.929. Según De Broglie, una partícula con cierta cantidad de movimiento se comporta como una onda. En tal sentido, el electrón tiene un comportamiento dual de onda y corpúsculo, pues tiene masa y se mueve a velocidades elevadas. Al comportarse el electrón como una onda, es difícil conocer en forma simultánea su posición exacta y su velocidad, por lo tanto, sólo existe la probabilidad de encontrar un electrón en cierto momento y en una región dada en el átomo, denominando a tales regiones como niveles de energía. La idea principal del postulado se conoce con el nombre de Principio de Incertidumbre de Heisenberg.
Radiactividad
a) Radiactividad Natural
En Febrero de 1.896, el físico francés Antoine Henri Becquerel investigando con cuerpos fluorescentes (entre ellos el Sulfato de Uranio y el Potasio), halló una nueva propiedad de la materia a la que posteriormente Marie Curie llamó "Radiactividad". Se descubre que ciertos elementos tenían la propiedad de emitir radiaciones semejantes a los rayos X en forma espontánea. Tal radiación era penetrante y provenía del cristal de Uranio sobre el cual se investigaba.
Marie Curie y Pierre Curie al proseguir los estudios encontraron fuentes de radiación natural bastante más poderosas que el Uranio original, entre estos el Polonio y el Radio.
La radiactividad del elemento no dependía de la naturaleza física o química de los átomos que lo componen, sino que era una propiedad radicada en el interior mismo del átomo.
Hoy en día se conocen más de 40 elementos radiactivos naturales, que corresponden a los elementos más pesados. Por arriba del número atómico 83, todos los núcleos naturales son radiactivos.
 Antoine Henri Becquerel |  Marie Curie y Pierre Curie |
b) Desintegraciones Alfa, Beta, Gamma
La radiactividad es un fenómeno que se origina exclusivamente en el núcleo de los átomos radiactivos. La causa que los origina probablemente se debe a la variación en la cantidad de partículas que se encuentran en el núcleo.
Cuando el núcleo atómico es inestable a causa del gran número de protones que posee (ocurre en los elementos más pesados, es decir con Z = 83 o superior), la estabilidad es alcanzada, con frecuencia, emitiendo una partícula alfa, es decir, un núcleo de Helio (₂He⁴) formado por dos protones y dos neutrones.
Cuando la relación de neutrones/protones en un núcleo atómico es elevada, el núcleo se estabiliza emitiendo un neutrón, o bien como ocurre con frecuencia, emitiendo una partícula beta, es decir, un electrón.
Cuando la relación de neutrones/protones es muy pequeña, debe ocurrir una disminución en el número de protones o aumentar el número de neutrones para lograr la estabilidad del núcleo. Esto ocurre con la emisión de un electrón positivo o positrón, o bien absorbiendo el núcleo un electrón orbital.
Los rayos gamma son ondas electromagnéticas de gran energía, muy parecidos a los rayos X, y en ciertas ocasiones se presentan cuando ocurre una desintegración de partículas beta, o bien una emisión de positrones. Por lo tanto, la radiación gamma no posee carga eléctrica y su naturaleza ondulatoria permite describir su energía en relación a su frecuencia de emisión.
c) Radiactividad Artificial
Al bombardear diversos núcleos atómicos con partículas alfa de gran energía, se pueden transformar en un núcleo diferente, por lo tanto, se transforma en un elemento que no existe en la naturaleza. Los esposos Irène Joliot-Curie y Frédéric Joliot, experimentando con tales procesos descubren la radiactividad artificial, pues se percatan que al bombardear ciertos núcleos con partículas procedentes de fuentes radiactivas estos se vuelven radiactivos. Si la energía de las partículas es adecuada, entonces puede penetrar en el núcleo generando su inestabilidad y por ende, induciendo su desintegración radiactiva.
Desde el descubrimiento de los primeros elementos radiactivos artificiales, el hombre ha logrado en el tiempo obtener una gran cantidad de ellos. Es clave en este proceso la aparición de los llamados aceleradores de partículas y de los reactores nucleares. Estos últimos son fuente importante de neutrones que son utilizados para producir gran variedad de radioisótopos.
Radiaciones
a) Radiaciones Ionizantes
Son radiaciones con energía necesaria para arrancar electrones de los átomos. Cuando un átomo queda con un exceso de carga eléctrica, ya sea positiva o negativa, se dice que se ha convertido en un ion (positivo o negativo).
Son radiaciones ionizantes los rayos X, las radiaciones alfa, beta, gamma y la emisión de neutrones. La radiación cósmica (proveniente del Sol y del espacio interestelar) también es un tipo de radiación ionizante, pues está compuesta por radiaciones electromagnéticas y por partículas con gran cantidad de energía. Es así como, los llamados rayos cósmicos blandos, se componen principalmente de rayos gamma, electrones o positrones, y la radiación cósmica primaria (que llega a las capas más altas de la atmósfera) se compone fundamentalmente de protones. Cuando la radiación cósmica interactúa con la atmósfera de la Tierra, se forman en ella átomos radiactivos (como el Tritio y el Carbono-14) y se producen partículas alfa, neutrones o protones.
Las radiaciones ionizantes pueden provocar reacciones y cambios químicos con el material con el cual interaccionan. Por ejemplo, son capaces de romper los enlaces químicos de las moléculas o generar cambios genéticos en células reproductoras.
b) Radiaciones No Ionizantes
Son aquellas que no son capaces de producir iones al interactuar con los átomos de un material.
Las radiaciones no ionizantes se pueden clasificar en dos grandes grupos: los campos electromagnéticos y las radiaciones ópticas.
Dentro de los campos electromagnéticos se pueden distinguir aquellos generados por las líneas de corriente eléctrica o por campos eléctricos estáticos. Otros ejemplos son las ondas de radiofrecuencia, utilizadas por las emisoras de radio en sus transmisiones, y las microondas utilizadas en electrodomésticos y en el área de las telecomunicaciones.
Entre las radiaciones ópticas se pueden mencionar los rayos láser, los rayos infrarrojos, la luz visible y la radiación ultravioleta. Estas radiaciones pueden provocar calor y ciertos efectos fotoquímicos al actuar sobre el cuerpo humano.
Autor: Giovanny Guillén Bustamante. Venezuela.
Editor: Ricardo Santiago Netto (Administrador de Fisicanet).