Problema nº 4 de calor de vaporización - TP10
Enunciado del ejercicio nº 4
¿Cuál es el calor de vaporización por gramo de agua a 25 °C?
Desarrollo
Datos:
Hf°(g) = -57,74184 kcal/mol (*)
Hf°(l) = -69,213792 kcal/mol (*)
Datos de la tabla de entalpías de formación la entalpía de cada sustancia:
Solución
Pide el calor de vaporización, no el calor latente de vaporización.
Podemos plantearlo como una ecuación termoquímica:
H₂O(l) ⟶ H₂O(g)
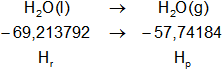
Planteamos la ecuación:
ΔH = Hₚ - Hᵣ
Reemplazamos por los datos y calculamos:
ΔH = -57,74184 kcal/mol - (-69,213792 kcal/mol)
ΔH = -57,74184 kcal/mol + 69,213792 kcal/mol
ΔH = 11,471952 kcal/mol
Hacemos la conversión de kcal/mol a kcal/g conociendo el mol de agua:
H₂O: 2·1,00797 g + 15,9994 g = 18,01534 g/mol
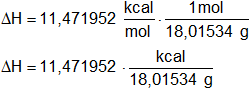
ΔH = 0,636787982 kcal/g
Respuesta: calor de vaporización por gramo de agua a 25 °C es 0,637 kcal.
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP10
- | Siguiente ›
Ejemplo, cómo calcular el calor de vaporización de un compuesto