Problema nº 5 de calor sensible, poder calorífico - TP11
Enunciado del ejercicio nº 5
La combustión de 5 g de coque eleva la temperatura de un litro de agua desde 10 °C hasta 47 °C. Calcular el poder calorífico del coque en kcal/g.
Desarrollo
Datos:
mc = 5 g
Vₐ = 1 l
t₁ = 10 °C
t₂ = 47 °C
cₑ = 1 cal/g·°C (calor específico del agua)
Fórmulas:
Q = m·cₑ·(t₂ - t₁)
Solución
El poder calorífico es la cantidad de calor desarrollado por la unidad de peso.
Hallamos la cantidad de calor necesario para calentar 1 litro de agua.
Aplicamos la ecuación de cantidad de calor para el agua:
Q = m·cₑ·(t₂ - t₁)
Convertimos las unidades:
Vₐ = 1 l ≅ 1 kg = mₐ
Convertimos las unidades de masa:
![]()
mₐ = 1.000 g
Reemplazamos por los valores y calculamos:
Q = 1 cal/g·°C·1.000 g·(47 °C - 10 °C)
Q = 1.000 cal/°C·37 °C
Q = 37.000 cal
La cantidad de calor necesario para calentar 1 litro de agua es Q = 37.000 cal.
Convertimos las unidades de calor:
![]()
Qₐ = 37 kcal
Luego, determinamos el poder calorífico del coque.
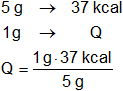
Pc = 7,4 kcal/g
Respuesta, el poder calorífico del coque es:
Pc = 7,4 kcal/g
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP11
- | Siguiente ›
Ejemplo, cómo calcular el poder calorífico