Problema nº 2 de la primera ley de Charles-Gay Lussac de los gases ideales, volumen de un gas - TP17
Enunciado del ejercicio nº 2
¿Hasta qué volumen se dilatará 1 litro de un gas si se le calienta desde 0 °C hasta la temperatura fisiológica de 37 °C, permaneciendo constante la presión?
Desarrollo
Datos:
V₁ = 1 l
t₁ = 0 °C
t₂ = 17 °C
Presión constante.
Fórmulas:
![]()
Solución
Aplicamos la primera ley de Charles-Gay Lussac de los gases ideales:
![]()
Despejamos V₂:
![]()
Convertimos las unidades de temperatura:
T₁ = 273 °C + 0 °C = 273 K
T₂ = 273 °C + 17 °C = 310 K
Reemplazamos por los datos y calculamos:
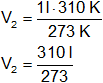
V₂ = 1,135531136 l
Resultado, el volumen de la masa de gas a 37 °C es:
V₂ = 1,136 l
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP17
- | Siguiente ›
Ejemplo de cómo determinar el volumen de un gas