Problema nº 4 de ley de Dalton, ley de las proporciones múltiples - TP05
Enunciado del ejercicio nº 4
Analizando tres compuestos de oxígeno y de carbono se hallaron los siguientes datos:
Compuesto 1: 27,28 % de C y 72,72 % O
Compuesto 2: 42,87 % de C y 57,13 % O
Compuesto 3: 52,96 % de C y 47,04 % O
Verificar que se cumple la ley de Dalton.
Solución
Aplicando la ley de Proust hallamos la masa de oxígeno que se combina con 1 g de carbono en cada compuesto. Tomamos el porcentaje de cada elemento equivalente a su masa considerando 100 % como 100 g de compuesto:
Compuesto 1
![]()
Compuesto 2
![]()
Compuesto 3
![]()
Comparamos los tres resultados dividiendo por el menor de ellos tenemos:
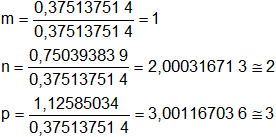
En este caso m, n y p son respectivamente 1; 2 y 3 (números enteros y pequeños)
Se verifica la ley de Dalton.
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP05
- | Siguiente ›
Ejemplo, aplicación de la ley de las proporciones múltiples