Problema nº 6 de átomos gramo - TP05
Enunciado del ejercicio nº 6
El aluminio tiene un peso atómico de 27 (u.m.a.), calcular:
a) La masa de un átomo gramo de aluminio.
b) Los átomos gramo que hay en 63 g de aluminio.
c) La masa de un átomo de aluminio.
Desarrollo
Datos:
Peso atómico Al = 27 (u.m.a.)
Masa Al = 63 g
1 átomo gramo ≡ 6,02·10²³ átomos (número de Avogadro)
Solución
a)
La masa de un átomo gramo es su peso atómico (u.m.a.) expresada en gramos, por lo tanto:
27 (u.m.a.) = 27 g
Respuesta a): la masa de un átomo gramo de aluminio 27 g
b)
Calculamos el número de átomos gramos:
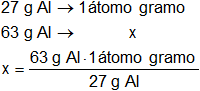
x = 2,33 átomos gramo
Respuesta b): en 63 g de aluminio hay 2,33 átomos gramo
c)
Calculamos la masa de un átomo de aluminio:
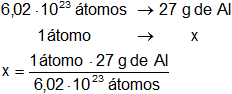
x = 4,485·10⁻²³ átomos de Al
Respuesta c): la masa de un átomo de aluminio es 4,485·10⁻²³ g
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP05
- | Siguiente ›
Ejemplo, cómo calcular los átomos gramo en una cantidad de sustancia