Los enlaces químicos en las moléculas
Las moléculas son agrupaciones estables de átomos unidos por un tipo de enlace químico que se denomina enlace covalente. Además de este enlace entre átomos las moléculas pueden unirse entre sí y organizarse en forma cristalina en el estado sólido. Las moléculas se representan mediante fórmulas químicas y mediante modelos.
Cuando dos o más átomos iguales o diferentes se unen entre sí formando una agrupación estable dan lugar a una molécula. Así, los gases hidrógeno (H₂) y oxígeno (O₂) están constituidos por moléculas diatómicas en las cuales los dos átomos componentes son esencialmente iguales; el agua está formada por moléculas que se producen por la unión de dos átomos de hidrógeno y uno de oxígeno (H₂O); en el gas metano (CH₄) cuatro átomos de hidrógeno se enlazan con uno de carbono para formar la correspondiente molécula.
Cada molécula de una sustancia compuesta constituye la porción más pequeña de materia que conserva las propiedades químicas de dicha sustancia. O en otros términos, las sustancias compuestas puras pueden ser consideradas como conjuntos de moléculas iguales. Cualquier proceso observable en o entre sustancias químicas puede interpretarse desde el punto de vista de lo que les sucede a sus átomos, a sus iones o a sus moléculas. Este fue el planteamiento mantenido por primera vez por John Dalton, que supuso una nueva orientación de la química y dio lugar, como uno de sus frutos, a la confección de la primera tabla de masas atómicas.
¿Cómo se forman las moléculas?
Ante la diversidad de elementos químicos existentes en la naturaleza cabe preguntarse cuál es la razón por la que unos átomos se reúnen formando una molécula y otros no; o de otra manera, por qué no toda molécula o agrupación de átomos imaginable tiene existencia real. Una primera respuesta puede hallarse en la tendencia observada en todo sistema físico a alcanzar una condición de mínima energía. Aquella agrupación de átomos que consiga reducir la energía del conjunto dará lugar a una molécula, definiendo una forma de enlace químico que recibe el nombre de enlace covalente.
Junto con esa idea general de configuración de energía mínima, otros intentos de explicación de este tipo de enlace entre átomos han sido planteados recurriendo a las características fisicoquímicas de las estructuras electrónicas de los átomos componentes.
La teoría de Lewis
El químico estadounidense Gilbert Newton Lewis (1.875 - 1.946) advirtió que el enlace químico entre átomos no podía explicarse como debido a un intercambio de electrones. Dos átomos iguales intercambiando electrones no alterarían sus configuraciones electrónicas; las ideas válidas para el enlace iónico no eran útiles para explicar de una forma general el enlace entre átomos. Sugirió entonces que este tipo de enlace químico se formaba por la comparación de uno o más pares de electrones o pares de enlace. Por este procedimiento los átomos enlazados alcanzaban la configuración electrónica de los gases nobles. Este tipo de configuración de capas completas se corresponde con las condiciones de mínima energía o máxima estabilidad características de la situación de enlace.
La teoría de Lewis, conocida también como teoría del octete por ser éste el número de electrones externos característicos de los gases nobles, puede explicar, por ejemplo, la formación de la molécula de yodo I₂:
![]()
Ambos átomos, que individualmente considerados tienen siete electrones en su capa externa, al formar la molécula de yodo pasan a tener ocho mediante la comparación del par de enalce.
Existen moléculas cuya formación exige la comparación de más de un par de electrones. En tal caso se forma un enlace covalente múltiple. Tal es el caso de la molécula de oxígeno O₂:
![]()
Para cuya formación se comparten dos pares de electrones. Representado cada par de electrones mediante una línea resulta:
![]()
Que indica más claramente la formación de un doble enlace.
En la molécula de nitrógeno N₂ sucede algo semejante, sólo que en este caso se han de compartir tres pares de electrones para alcanzar el octete, con la formación consiguiente de un triple enlace:
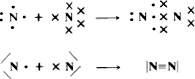
Esta explicación puede extenderse al caso de las moléculas formadas por átomos de elementos no metálicos diferentes entre sí, tales como HCl, NH₃, H₂O o CO₂ por ejemplo:
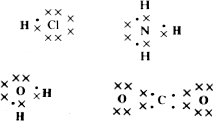
Lewis contempló la posibilidad extrema de que los pares electrónicos de enlace fueran aportados por un sólo átomo.
Tal es el caso de ion, NH₄⁺, en el cual el átomo de nitrógeno aporta el par de electrones al enlace con el ion H⁺:
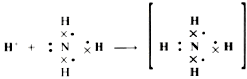
Este tipo de enlace covalente se denomina coordinado o dativo.
Los subíndices que aparecen en las fórmulas químicas de compuestos covalentes expresan el número de átomos que se combina para formar una molécula y están, por tanto, relacionados con la capacidad de enlace de cada uno de ellos, también llamada valencia química. Según la teoría de Lewis, la configuración electrónica de la capa externa condiciona dicha capacidad y es la responsable del tipo de combinaciones químicas que un determinado elemento puede presentar.
La teoría del enlace de valencia
La superación del modelo de Bohr y el desarrollo del modelo atómico de la mecánica cuántica tuvo una clara repercusión en las ideas sobre el enlace químico en general y sobre el covalente en particular. Uno de los enfoques mecanocuánticos del enlace covalente se conoce como teoría del enlace de valencia y permite comprender en términos no sólo de energías, sino también de fuerzas, el fenómeno del enlace entre átomos.
La formación del enlace covalente simple tiene lugar cuando los orbitales correspondientes a dos electrones desapareados de átomos diferentes se superponen o solapan, dando lugar a una región común en la cual los dos electrones con espines opuestos, tal y como exige el principio de exclusión de Pauli, ocupan un mismo orbital. Ese par compartido constituye el elemento de enlace entre los dos átomos.
Así, por ejemplo, cuando dos átomos de H se aproximan suficientemente, existe una disposición en la cual sus nubes electrónicas están parcialmente solapadas y para la que la energía potencial del conjunto es mínima, constituyendo, pues, una situación de enlace. En términos electrónicos puede afirmarse que el orbital 1s de cada átomo de hidrógeno, semiocupado por su electrón correspondiente, es completado por el electrón del otro átomo de hidrógeno. Los dos electrones con espines opuestos de este par, son atraídos entonces por cada uno de los núcleos, constituyendo el par de enlace. La existencia de este par común es lo que determina que los núcleos estén ligados entre sí con las limitaciones que, en cuanto a proximidad, imponen las fuerzas de repulsión nuclear.
La primitiva idea de comparación de electrones de Lewis sigue, de algún modo, presente en la teoría del enlace de valencia, aunque se abandona la regla del octete y se sustituye por la condición de que dos electrones desapareados puedan ocupar un mismo orbital. El número de enlaces covalentes posible depende, entonces, del número de electrones desapareados presentes en el átomo correspondiente o en algún estado excitado previo a la formación de la molécula.
Iones y moléculas
La polaridad eléctrica de las moléculas
El hecho de que en una molécula los átomos enlazados no sean iguales, hace que el grado de comparación electrónica no sea el mismo para ambos. Cada elemento no metálico presenta una tendencia diferente a captar electrones (electronegatividad). En una unión covalente el átomo más electronegativo atraerá con mayor intensidad al par o pares de enlace y esa nube electrónica compartida se desplazará hacia dicho átomo alejándose del otro. Por tal motivo la distribución de carga en la molécula resulta asimétrica y ésta se convierte en un pequeño dipolo eléctrico con una región negativa y otra positiva. Esta circunstancia se hace tanto más patente cuanto mayor es la diferencia entre la electronegatividad de los átomos enlazados. Se dice entonces que el enlace covalente es polar, lo cual significa que se aproxima, en cierta medida, a un enlace de tipo iónico. Entre un enlace covalente puro (no polar) y un enlace iónico puro existen, pues, formas intermedias en las que el enlace real participa de las características de ambos tipos extremos e ideales de enlace químico.
Las moléculas polares se comportan de una forma parecida a como lo hacen los iones. La molécula de agua es un caso típico de molécula polar en la cual el carácter electronegativo del átomo de oxígeno respecto del hidrógeno hace que los dos pares de electrones de enlace estén desplazados hacia su núcleo. De una forma aproximada se puede decir que la mayor carga positiva del núcleo de oxígeno (Z = 8) respecto del de hidrógeno (Z = 1) atrae hacia sí los pares de electrones compartidos en el enlace, de modo que éstos se hallan moderadamente desplazados hacia el oxígeno. Esta asimetría en la distribución de las cargas en cada uno de los enlaces H—O, confiere a éstos una cierta polaridad eléctrica. Es decir, el átomo de oxígeno se encuentra sobrecargado negativamente en tanto que los dos átomos de hidrógeno aparecen cargados positivamente, aun cuando la molécula en su conjunto sea eléctricamente neutra. A causa del carácter polar del enlace oxígeno-hidrógeno, la molécula de agua se convierte en un dipolo eléctrico.
El fenómeno de la hidratación
El carácter dipolar de la molécula de agua es el responsable de diferentes propiedades fisicoquímicas de esta sustancia y, en particular, de su poder como disolvente de compuestos iónicos. Cuando un cristal iónico de cloruro de sodio (NaCl) se sumerge en agua las moléculas de ésta, al ser móviles, son atraídas por los centros eléctricos fijos del cristal, orientando sus polos positivos hacia los iones negativos de la red y viceversa. Estas fuerzas atractivas ion-dipolo debilitan los enlaces entre los iones de la red cristalina, con lo que su estructura comienza a desmoronarse y al cabo de un cierto tiempo sobreviene la disolución total del cristal.
Cada ion en libertad es rodeado completamente por moléculas de agua orientadas de forma diferente según sea la polaridad de aquél. Se dice entonces que el ion está hidratado y el proceso de formación de esta capa de moléculas de agua en torno suyo se denomina hidratación. Cuando este fenómeno implica la intervención de moléculas polares diferentes del agua recibe el nombre genérico de solvatación.
La polaridad de las moléculas y el momento dipolar
No sólo la electronegatividad desempeña un papel importante en el carácter polar o no polar de una molécula, sino también su geometría. En el caso del agua, los dos dipolos correspondientes a sus enlaces dan una suma no nula. El efecto de la polarización de un enlace puede representarse en términos de fuerzas. Componiendo vectorialmente ambas acciones dipolares resulta un efecto conjunto no nulo responsable de los fenómenos de hidratación anteriormente descritos.
Sin embargo, es posible que una molécula posea enlaces muy polarizados, pero que en conjunto se comporte como apolar. Tal es el caso del trifluoruro de boro (BF₃). Su geometría es plana, estando los átomos de flúor situados en los vértices de un triángulo equilátero y el átomo de boro en su centro geométrico. La composición vectorial de los tres dipolos individuales da un efecto global nulo. La magnitud física que da idea de la polaridad de la molécula en su conjunto recibe el nombre de momento dipolar.
Sólidos moleculares
Sólidos formados por moléculas no polares
Las moléculas no polares pueden ordenarse de forma regular, dando lugar, a temperaturas suficientemente bajas, a sólidos cristalinos. Ello implica la existencia de ciertos tipos de fuerzas intermoleculares que a pesar de ser muy débiles poseen un efecto ordenador que hace posible la formación del cristal. El hecho de que sustancias moleculares tales como Cl₂, H₂, CO₂, etc., sean blandas y posean muy bajos puntos de solidificación es precisamente consecuencia de la debilidad de tales fuerzas, las cuales son capaces de vencer los efectos disgregadores de la energía térmica sólo a muy bajas temperaturas. Estas fuerzas de interacción molecular reciben el nombre de fuerzas de Van der Waals.
La naturaleza de las fuerzas de Van der Waals puede explicarse del siguiente modo: aun aquellas moléculas que no poseen un carácter dipolar permanente pueden convertirse en dipolos durante brevísimos intervalos de tiempo; esto es consecuencia de los cambios que se producen en las distribuciones de carga en el interior de los átomos y que implican acumulaciones transitorias en ciertos sitios. Las interacciones que resultan entre estos dipolos instantáneos y fluctuantes son la causa de que aparezcan estas débiles fuerzas de atracción entre moléculas no polares que dan lugar a sólidos blandos que pueden pasar a estado líquido e incluso directamente a vapor con facilidad.
Sólidos formados por moléculas polares
Las moléculas polares pueden unirse entre sí para formar estructuras cristalinas típicas del estado sólido, comportándose de una forma parecida a como lo hacen los iones en un cristal iónico. El resultado es la formación de ordenaciones reticulares o redes cristalinas cuyos puntos de fusión o de ebullición y cuya resistencia mecánica resultan superiores a las que cabría esperar si se tratase de moléculas no polares. Son las fuerzas electrostáticas por una parte y la organización reticular por otra lo que les confiere esas propiedades.
El punto de fusión o la dureza del cristal están relacionados con la solidez de la estructura y ésta a su vez con la intensidad de las fuerzas que mantienen unidos a sus componentes. El comportamiento de los sólidos de moléculas polares es, en este sentido, inferior al de los sólidos iónicos.
Un tipo de enlace intermolecular especialmente interesante se presenta cuando las moléculas en cuestión son fuertemente polares y contienen, además, algún átomo de hidrógeno. Se conoce con el nombre de enlace de hidrógeno o enlace por puentes de hidrógeno porque el átomo de hidrógeno hace de puente de unión entre las moléculas. El agua constituye un ejemplo de sustancia en la que la presencia de puentes de hidrógeno es importante. Cada átomo de hidrógeno con su carga positiva efectiva puede atraer o ser atraído por un átomo de oxígeno de otra molécula de agua. Estas interacciones hacen que por debajo de los 0 °C de temperatura se genere una estructura sólida cristalina: es el hielo.
En estado sólido las moléculas de agua se ordenan tetraédricamente, situándose los átomos de oxígeno en los centros de los tetraedros, en tanto que los cuatro vértices son ocupados dos por los átomos de hidrógeno propios y otros dos por átomos de hidrógeno de otras moléculas ligados electrostáticarnente al átomo de oxígeno central. A causa de esta ordenación, cada molécula de agua aparece rodeada únicamente por otras cuatro enlazadas entre sí por estas fuerzas de atracción intermolecular. La estructura cristalina así formada es muy abierta y voluminosa, es decir, poco densa.
Cuando por efecto de un aumento en la temperatura se inicia la fusión del hielo algunos enlaces entre moléculas por puentes de hidrógeno se rompen, se desmorona la estructura tetraédrica y las moléculas de agua se apiñan unas al lado de otras en un agrupamiento más compacto. Por esta razón, y en contra de lo que es habitual, el agua líquida es más densa que el hielo. Este proceso de ruptura de enlaces de hidrógeno aumenta con la temperatura, por lo que de 0 °C a 4 °C el agua líquida aumenta de densidad. A partir de los 4 °C la dilatación producida por el incremento térmico es ya capaz de contrarrestar el efecto anterior de signo opuesto, con lo que la densidad del agua comienza a disminuir con la temperatura. El agua presenta, pues, un máximo de densidad a los 4 °C, lo cual tiene una considerable importancia en la naturaleza al hacer posible el mantenimiento de la vida en medios subacuáticos en condiciones exteriores de bajas temperaturas.
La masa de las moléculas
Fórmulas químicas
Las sustancias compuestas se representan mediante una combinación de símbolos químicos de los elementos que las constituyen. Esta forma de representación, introducida por el químico sueco Jöns Jacob Berzelius (1.779 - 1.848), posee un doble significado, pues no sólo indica qué elementos están presentes en un compuesto dado, sino también en qué proporción los átomos respectivos participan en la formación de su molécula. Cada símbolo en una fórmula química equivale a un átomo de la sustancia simple correspondiente. Los subíndices que pueden aparecer en una fórmula, hacen referencia al número de átomos de cada elemento.
Si se toma en consideración la masa de los átomos la fórmula de una combinación química expresa, además, la proporción en masa en la que los elementos en cuestión intervienen en la formación de una sustancia compuesta dada.
Así, la fórmula del amoníaco, NH₃, indica que esta sustancia resulta de la combinación de hidrógeno y nitrógeno a razón de tres átomos de hidrógeno por cada uno de nitrógeno, o en otros términos, en la proporción de 3·1,008 gramos de hidrógeno por cada 1·14,007 gramos de nitrógeno.
Este tipo de fórmula, llamada también fórmula empírica o molecular, no indica, sin embargo, nada sobre la estructura de la molécula, es decir, sobre la forma en que sus átomos componentes y los enlaces entre ellos se distribuyen en la molécula. Así, la fórmula empírica del agua H₂O podría corresponder a cualquiera de las siguientes configuraciones de sus átomos componentes:
![]()
De estas tres la única que es conforme a los resultados experimentales es la tercera. Cuando interesa reflejar las orientaciones de los enlaces, la fórmula estructural, que es el nombre que recibe este tipo de fórmula química, se aproxima bastante a un modelo molecular en el que se reproducen a escala los átomos, la longitud de los enlaces y sus ángulos respectivos. En tal caso la fórmula del agua deberá representarse en la forma:
![]()
Ya que los dos enlaces H—O forman entre sí un ángulo de 105°.
La masa de una molécula y de un mol
Las masas moleculares se expresan en unidades de masa atómica (u), las cuales, por su tamaño, resultan apropiadas a este tipo de cantidades. La masa de una molécula en u será la suma de las masas de los diferentes átomos que la componen y que aparecen recogidos en la fórmula molecular correspondiente. Así la masa molecular del metano (CH₄) será 4·M(H) + 1·M(C), siendo M(H) y M(C) las masas atómicas de los átomos de hidrógeno y carbono respectivamente; es decir, M(CH₄) = 4·1,008 + 12,011 = 16,043 u.
Como cantidad de sustancia, un mol de un compuesto dado es igual a un mol de sus moléculas, lo que equivale, de acuerdo con la definición de mol, a Na moléculas, siendo NA = 6,023·10²³ el número de Avogadro. Dado que 1 gramo equivale a NA u, el mismo número que indica la masa de una molécula en unidades de masa atómica indica también el valor de su mol expresado en gramos. Así un mol de metano equivale a:
NA·16,043 u = 16,043 NA u = 16,043 g
A la masa expresada en gramos que corresponde a un mol de una sustancia compuesta se la denomina también molécula-gramo.
Aplicación del concepto mol
El cloroformo es una sustancia que se emplea como anestésico y cuya fórmula química es:
![]()
Calcular su masa molecular en u y el valor de su mol en gramos. ¿Cuántos moles de sustancia estarán contenidos en una muestra de 15,00 gramos? ¿Y cuántas moléculas? ¿Y cuántos átomos de cloro? Determinar el porcentaje en masa de cloro que contiene el cloroformo.
La masa molecular M es la suma de las masas atómicas, de modo que:
M(CHCl₃) = M(C) + M(H) + 3·M(Cl) = 12 + 1 + 3·35,5 = 119,5 u
Por tanto,
1 mol de CHCl₃ = 119,5 gramos
El número de moles de CHCl₃ contenidos en 15,00 g de sustancia se obtendrá dividiendo la masa en gramos por el número de gramos por mol:
| n° de moles = | masa (g) |
| n° de g/mol |
| n° de moles = | 15,00 |
| 119,5 |
n° de moles = 0,126 moles
Dado que cada mol de CHCl₃ equivale a NA moléculas, resultará:
n° de moléculas = n° moles·NA = 0,126·6,023·10²³ = 0,759·10²³
Por cada molécula de CHCl₃ hay tres átomos de cloro, de modo que en esta sustancia se cumplirá:
n° de átomos (Cl) = n° moléculas (CHCl₃)·3 = 0,759·10²³·3 = 2,277·10²³
Finalmente el tanto por ciento en masa de cloro se calculará a partir de la contribución del cloro a la masa molecular. De las 119,5 u del CHCl₃, 3·35,5 = 106,5 proceden del cloro, por tanto:
| % de Cl = | 106,5·100 |
| 119,5 |
% de cloro = 89,12 %
Editor: Ricardo Santiago Netto (Administrador de Fisicanet).
¿Qué dice la regla de Lewis? ¿Qué es una estructura de Lewis y para qué se utiliza?