Guía nº 2 de ejercicios de enlaces químicos
Resolver los siguientes ejercicios
� Ver resolución de los ejercicios al pie de la página
Problema nº 1
Esquematizar las uniones químicas formadas entre los átomos de:
a) Flúor y litio al formar fluoruro de litio LiF.
b) Cloro y sodio al formar cloruro de sodio NaCl.
Problema nº 2
Empleando sólo los electrones de valencia y utilizando puntos, asteriscos o cualquier otro símbolo, esquematizar las estructuras electrónicas de las siguientes sustancias:
a) H₂S
b) C₂H₆
c) CH₂O
d) HCN
e) C₂H₆O
f) CH₅N
g) CHCl₃
h) CH₃OH
i) CH₃Cl
j) BF₃
Problema nº 3
¿Cuál de las siguientes moléculas contienen enlaces polares? ¿Qué moléculas son polares? Justificar:
a) C₂H₆
b) BF₃
c) CH₃OH
d) CH₄
e) CH₃Br
f) CCl₂F₂
g) CCl₄
h) HI
i) CO₂
j) C₂H₅OC₂H₅
Problema nº 4
¿En cuál de los halogenuros de hidrógeno será más polar el enlace entre el halógeno y el hidrógeno? ¿Cuál el menos polar? Justificar:
Responder el siguiente cuestionario
Pregunta nº 1
Existe unión electrovalente o iónica cuando:
a) Dos átomos comparten un par de electrones.
b) Un átomo pierde uno o más electrones y otro/s átomo/s lo o los ganan.
c) En un compuesto hay iones positivos e iones negativos.
d) Todas las respuestas son correctas.
Pregunta nº 2
Los compuestos con uniones iónicas tienen las siguientes características:
a) Forman moléculas volátiles.
b) Conducen la corriente eléctrica fundidos o en solución en determinados solventes.
c) Forman cristales de alto punto de fusión.
d) Conducen la corriente eléctrica en estado sólido.
Pregunta nº 3
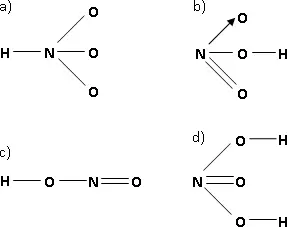
¿Cuál de las siguientes fórmulas desarrolladas corresponde al ácido nítrico?
Autor: Ricardo Santiago Netto. Argentina